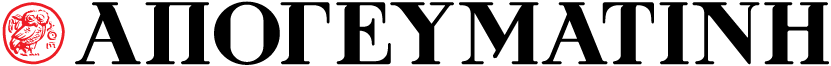Ιδιαίτερη προσοχή πρέπει να δώσουν οι πλέον ευπαθείς ασθενείς της χώρας μας σε προειδοποίηση την οποία εξέδωσε ο Εθνικός Οργανισμός Φαρμάκων (ΕΟΦ) για σκευάσματα («φάρμακα») που κυκλοφορούν ανορθόδοξα και στη χώρα μας και μπορεί να προκαλέσουν πολύ σοβαρές βλάβες στην υγεία τους.
Συγκεκριμένα, ο Ευρωπαϊκός Οργανισμός Φαρμάκων (European Agency Medicines, EMA) και η Οργάνωση των Επικεφαλής των Εθνικών Οργανισμών Φαρμάκων της Ευρωπαϊκής Ένωσης (Heads of Medicines Agencies, HMA) προειδοποιούν το κοινό για τους κινδύνους των μη αδειοδοτημένων φαρμάκων προηγμένων θεραπειών (ATMP). Τα ATMP είναι φάρμακα που βασίζονται σε κύτταρα, ιστούς ή γονίδια.
Όταν τα φάρμακα προηγμένων θεραπειών (ATMP) είναι αδειοδοτημένα (δηλαδή η χρήση τους έχει εγκριθεί είτε από τον EMA είτε από την αρμόδια εθνική αρχή – ΕΟΦ για την Ελλάδα) μπορούν να προσφέρουν σημαντικά οφέλη, καθώς ακολουθούν τις κατευθυντήριες γραμμές που έχουν θεσπιστεί από την ΕΕ, προκειμένου να διασφαλιστεί ότι πληρούν τα απαιτούμενα πρότυπα ποιότητας, ασφάλειας και αποτελεσματικότητας, ώστε να χορηγηθούν σε ασθενείς.
Ωστόσο, έχει διαπιστωθεί η διάθεση σε χώρες της ΕΕ μη αδειοδοτημένων ATMP από μεμονωμένα άτομα ή εταιρείες ή κλινικές, μεταξύ των οποίων θεραπείες δενδριτικών κυττάρων για τον καρκίνο.
Εδώ είναι που πρέπει να δώσουμε όλοι μας ιδιαίτερη προσοχή: Τα μη αδειοδοτημένα φάρμακα προηγμένων θεραπειών δεν είναι ελεγμένα ως προς την ασφάλεια, την αποτελεσματικότητα και την ποιότητά τους. Κατά συνέπεια, η χρήση τους εγκυμονεί σοβαρούς κινδύνους, καθώς μπορεί να επιφέρουν σοβαρές και ανεπιθύμητες βλάβες, χωρίς ταυτόχρονα να παρέχουν οφέλη, αφήνοντας τους ασθενείς όχι μόνο ακάλυπτους έναντι της νόσου για την οποία αναζητούν θεραπεία, αλλά και επιβαρυμένους με επιπλέον προβλήματα υγείας. Επιπρόσθετα, οι θεραπείες αυτές συνοδεύονται από σημαντικό οικονομικό κόστος.
Ο ΕΟΦ αναφέρει, επίσης, ότι όσοι προωθούν τέτοια φάρμακα το κάνουν ως εξής:
– Ο πάροχος διαθέτει το προϊόν στην αγορά ως πειραματικό, αλλά το χορηγεί εκτός εγκεκριμένης κλινικής δοκιμής.
– Ο πάροχος δεν επιβεβαιώνει ότι το προϊόν έχει λάβει άδεια κυκλοφορίας από τον ΕΜΑ ή ότι χορηγείται στο πλαίσιο εγκεκριμένης κλινικής δοκιμής.
– Το προϊόν προωθείται σε ιστοσελίδες ή σε μέσα κοινωνικής δικτύωσης ως τελευταία ελπίδα, στοχεύοντας στις ανησυχίες των ασθενών και των οικογενειών τους (ωστόσο μπορεί και να προτείνεται απευθείας στον πάσχοντα ή στους οικείους του από μεμονωμένο άτομο ή ιατρείο ή κλινική).
Εφημερίδα Απογευματινή
Διαβάστε επίσης: